Нейробластома – злоякісна пухлина, що розвивається з наднирникових залоз або рідше з екстраадреналового симпатичного стовбура, що розташовується заочеревинному просторі, грудній клітці та в певних ділянках шиї. Діагноз підтверджується по результатам біопсії. Лікування може включати хірургічне видалення, хіміотерапію, променеву терапію, високодозовану хіміотерапію з трансплантацією стовбурових клітин, застосування цис-ретиноєвої кислоти та імунотерапію.
Нейробластома є найпоширенішою формою раку у дітей. Майже 90% нейробластом виникають у дітей до 5 років. Більшість таких пухлин виникають спонтанно, але 1-2%, очевидно, передаються по спадковості.

Нейробластоми можуть локалізуватися в черевній порожнині (близько 65%), грудній клітці (15–20%), шиї, тазі або інших місцях. Нейробластома вкрай рідко зустрічається як первинний рак центральної нервової системи.
Більшість нейробластом продукують гормони катехоламіни і можуть бути запідозрені у випадку підвищеного вмісту в сечі продуктів розпаду катехоламінів. Нейробластоми зазвичай не викликають тяжку артеріальну гіпертензію, тому що ці пухлини, як правило, не виділяють адреналін.
Нейробластоми – це незрілі недиференційовані злоякісні пухлини. Гангліонейробластоми є проміжними пухлинами, а гангліоневроми – повністю диференційованими доброякісними варіантами нейробластоми. Разом вони складають групу пухлин з клітин нервового гребня.
40-50% дітей мають місцеворозповсюджене захворювання на момент встановлення діагнозу, 50-60% на момент встановлення діагнозу уже мають метастази. Нейробластома може метастазувати у кістковий мозок, кістки, печінку, лімфатичні вузли або, рідше, у шкіру чи головний мозок. Метастази кісткового мозку можуть призвести до анемії та/або тромбоцитопенії.
Нейробластома – це важке захворювання з серйозним прогнозом, але при вчасній діагностиці та грамотному сучасному комплексному лікуванні – цілком виліковне. Основне – знайти спеціаліста, який має успішний досвід ведення пацієнтів з нейробластомами. Саме такі лікарі працюють у відділенні дитячої онкології багатопрофільного медичного центру Маймонідес. Наша клініка тісно співпрацює з найкращими ізраїльськими онкологічними центрами. Кожен окремий випадок захворювання ведеться спільно лікуючим лікарем, завідуючим відділення та відповідальним онкологом безпосередньо з Ізраїлю. Завдяки злагодженій роботі такої професійної команди нам вдається досягти успіхів навіть у найскладніших ситуаціях.
Медичний центр Маймонідес працює під патронажем благодійного фонду “КЕРЕН ОР ДЛЯ НАШОЇ ДИТИНИ”, тому всі наші пацієнти, а особливо важкохворі діти, мають можливість отримати фінансову допомогу на необхідне лікування.
Всі наші лікарі мають чудову теоретичну підготовку та багатий практичний досвід, більшість з них неодноразово стажувалися на базі найкращих онкологічних центрів світу. У своїй практиці наші фахівці керуються сучасними клінічними рекомендаціями та світовими протоколами лікування, тому в якості надання медичних послуг можна не сумніватися. Разом з цим підхід до кожного маленького пацієнта індивідуальний. Лікар при складанні плану обстеження та схеми терапії враховує всі особливості як зі сторони пацієнта, так і з боку його захворювання. Це дозволяє створити найефективнішу персоналізовану схему лікування для кожної окремої дитини, що в подальшому лише позитивно відображається на довгостроковому прогнозі.
Медичний центр Маймонідес забезпечує мультидисциплінарний підхід до кожного клінічного випадку. Тобто допомогу одній дитині з нейробластомою надає ціла команда профільних спеціалістів – онкологи, хірурги, нейрохірурги, торакальні хірурги, променеві терапевти, хіміотерапевти, реабілітологи, психологи та інші вузькі фахівці у разі необхідності. Таким чином в одному закладі можна отримати всі необхідні медичні процедури, починаючи з етапу діагностики, завершуючи комплексним лікуванням та необхідним обсягом реабілітаційних заходів. Більшість необхідних маніпуляцій можна отримати в межах України. Якщо певне рідкісне діагностичне обладнання або вузький спеціаліст відсутні – пацієнт за згодою батьків скеровується в дочірні медичні центри або ізраїльські клініки-партнери, де гарантовано будуть надані всі необхідні медичні послуги.
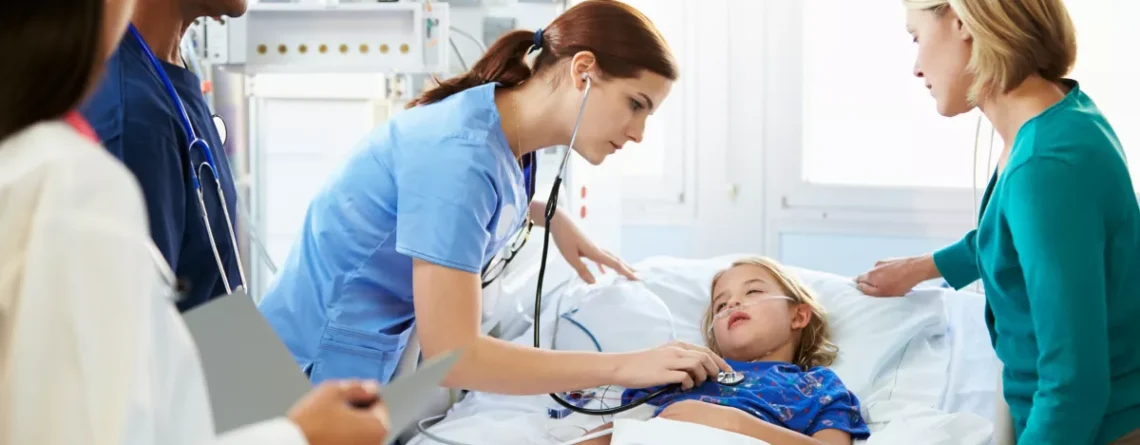
Причини та симптоми нейробластоми
На жаль, істинні причини розвитку нейробластоми на сьогодні невідомі. Певні чинники можуть підвищувати ризик розвитку пухлини. Такі новоутворення частіше розвивається в дітей віком до 5 років, також дещо частіше хворіють хлопчики, ніж дівчатка.
У невеликої кількості пацієнтів (1-2%) відзначається спадкова нейробластома. Цей різновид захворювання може передаватися з покоління в покоління. Спадкова нейробластома найчастіше виникає внаслідок мутацій в генах ALK або PHOX2B. У пацієнтів із спадковою нейробластомою ймовірність передачі захворювання своїм дітям становить 50%.
Симптоми нейробластоми залежать від локалізації первинного вогнища та поширеності пухлини (стадії). Найчастішими патологічними ознаками є біль у животі, дискомфорт і відчуття швидкого насичення під час їжі внаслідок наявності об’ємного утворення в черевній порожнині.
Деякі ознаки з’являються в результаті метастазування. Вони включають болі в кістках через ретробульбарні метастази, періорбітальні екхімози (крововиливи) та екзофтальм через ретробульбарні метастази, здуття живота та проблеми з диханням, пов’язані з метастазами в печінці.
У дітей також можуть бути виражені осередкові неврологічні симптоми або порушення рухової функції (парез, параліч) через безпосереднє поширення ракових клітин в хребетний канал. Пухлини в ділянці шиї або верхній частині грудної клітки можуть спричинити розвиток синдрому Горнера (птоз, міоз, ангідроз – опущення повіки, звуження зіниці, порушення потовидільної функції на одній частині обличчя). У них можуть бути виражені також різноманітні паранеопластичні синдроми.

Методи діагностики нейробластоми
Вивчення історії хвороби та медичний огляд для отримання відомостей про симптоми, загальний стан здоров’я, перенесені захворювання, сімейний анамнез та інші фактори ризику – це початковий та обов’язковий етап діагностичної програми, після якого спеціаліст складе список уточнюючих обстежень лабораторних та інструментальних.
Серед необхідних лабораторних аналізів призначають клінічний аналіз крові та проби для оцінки функції нирок та печінки.
При діагностиці нейробластоми лікарі досліджують вміст ванілілмигдальної кислоти (ВМК) та гомованілінової кислоти (ГВК) у сечі. Ці речовини утворюються при розпаді гормонів симпатичної нервової системи – катехоламінів. Катехоламіни виділяються нейробластомами в кров. Таким чином, у дітей з нейробластомою часто спостерігається високий рівень цих речовин. Крім того, дослідження рівня цих речовин можна використовувати для контролю відповіді на лікування.
Неврологічне обстеження для оцінки різних аспектів роботи мозку та функції нервової системи, включаючи пам’ять, зір, слух, м’язову силу, рівновагу, координацію та рефлекси – обов’язковий етап діагностики.
Методи діагностичної візуалізації, які використовуються при діагностиці нейробластоми:
- Рентгенографія.
- УЗД.
- Комп’ютерна томографія (КТ).
- Магнітно-резонансна томографія (МРТ) дозволяє отримувати деталізовані зображення. Ці зображення допомагають лікарям краще візуалізувати пухлину та розробити план лікування.
- Для пошуку вогнищ захворювання в інших частинах тіла (метастазів) використовують візуалізацію всього тіла, включаючи остеосцинтиграфію, ПЕТ-КТ або сканування з МЙБГ (метайодбензилгуанідин).
- Пункція та біопсія кісткового мозку для виявлення ракових клітин у кістковому мозку.
- Часто для встановлення правильного діагнозу потрібна біопсія пухлини. Під час біопсії лікар отримує невелику кількість тканини з пухлини. Потім клітини вивчають під мікроскопом, щоб з’ясувати, що це за пухлина, які її особливості. Залежно від розташування пухлини може знадобитися інцизійна біопсія або пункційна.
Всі матеріали після біопсії ми відправляємо для ревізії в найкращі патогістологічні лабораторії світу (Ізраїль, США, Німеччина), де їх переглядає кваліфікований спеціаліст. Завдяки таким подвійним перевіркам ми точно впевнені в правильності діагнозу та подальшій вибраній лікувальній тактиці. Також після біопсії проводять інноваційні молекулярно-генетичні тести, щоб виявити особливості пухлинних клітин, що дозволяє підібрати найефективнішу схему лікування.
Одним із таких тестів є комплексне геномне профілювання пухлини Foundation One. Це лінійка генетичних тестів для індивідуального підбору таргетного лікування онкологічного захворювання. Це єдині тести, схвалені до застосування FDA (Управління США з контролю якості харчових продуктів та лікарських засобів). Дослідження Foundation One ґрунтується на глибокому аналізі геному пухлини, що дозволяє виявити клінічно значущі мутації та потенційно розширити терапевтичні опції для кожного пацієнта.

Прогноз при нейробластомі
Ймовірність одужання при нейробластомі залежить від кількох факторів:
- Вік дитини на момент встановлення діагнозу (молодший вік пов’язаний з більш сприятливими наслідками).
- Особливості пухлини, включаючи гістологічні характеристики, генні зміни та швидкість росту злоякісних клітин.
- Група ризику: низька, проміжна або висока.
- Розташування пухлини.
- Розповсюдження раку на лімфатичні вузли або інші частини тіла (метастазування).
- Можливість повного видалення пухлини хірургічним шляхом.
- Реакція пухлини на лікування.
- Наявність рецидиву захворювання та скільки часу пройшло до рецидиву.
Існує кілька способів класифікації нейробластоми. Згідно з міжнародною системою стадіювання нейробластом (INSS), пухлина класифікується з урахуванням її розташування, поширення захворювання та результату хірургічної операції:
- Стадія 1. Пухлина обмежена однією анатомічною ділянкою та повністю видаляється в ході хірургічної операції.
- Стадія 2. 2A: пухлина знаходиться тільки в одній області, але не повністю видаляється в ході хірургічної операції. 2B: пухлина може бути повністю видалена в ході хірургічної операції, але ракові клітини виявляються у сусідніх лімфатичних вузлах.
- Стадія 3. Пухлина не може бути повністю видалена в ході хірургічної операції і захворювання поширюється на інший бік тіла в лімфатичні вузли або інші тканини. Якщо пухлина розташовується по серединній лінії (в центрі) тіла, спостерігається поширення пухлини на лімфатичні вузли або тканини з обох сторін.
- Стадія 4. Пухлина поширилася у віддалені лімфатичні вузли, кістки, кістковий мозок, печінку, шкіру та/або інші органи. 4S: дитина молодша 1 року. Первинна пухлина розташовується лише на місці початку зростання (1 чи 2 стадія). Пухлина поширюється лише на шкіру, печінку чи кістковий мозок (невеликі кількості клітин).
Міжнародна система стадіювання груп ризику нейробластоми (INRGSS) класифікує захворювання без урахування результатів хірургічної операції. Система враховує розташування пухлини та поширення захворювання. Для визначення стадії використовують методи діагностичної візуалізації:
- Стадія L1 (локалізована). Пухлина не поширюється далі первинного вогнища. Відсутнє вростання у життєво важливі анатомічні структури. Захворювання обмежене однією ділянкою тіла, наприклад, шиєю, грудною клітиною, животом або тазом.
- Стадія L2 (локалізована). За допомогою методів діагностичної візуалізації виявлено наявність одного чи кількох візуально визначених факторів ризику. Можливе поширення пухлини на прилеглі структури або дві області тіла.
- Стадія М (метастатична). Пухлина поширилася на віддалені частини тіла. Сюди відносяться всі пухлини з метастазами, крім пухлин класифікованих як MS.
- Стадія MS (метастатична). Для дітей віком до 18 місяців: пухлина з метастазами, які обмежені печінкою, шкірою та/або невеликою частиною кісткового мозку.
При класифікації нейробластоми та плануванні лікування лікарі також використовують групи ризику. Високий ризик означає високу ймовірність рецидиву пухлини. Пацієнти з нейробластомою високого ризику потребують більш інтенсивної терапії.
Чинники, що визначають групу ризику:
- Вік.
- Стадія.
- Гістологічні характеристики пухлини.
- Статус MYCN.
- Хромосомний набір клітин пухлини.
- Індекс ДНК — оцінка вмісту ДНК у пухлинній клітині, порівняно із вмістом ДНК у нормальній клітині.
Біологічні та гістологічні особливості нейробластом впливають на результати лікування. Певні генетичні особливості пухлини, включаючи ампліфікацію гена MYCN, пов’язані з підвищеним ризиком. Гістологічні характеристики пухлини (вид клітин під мікроскопом) також впливають на ризик рецидиву.
Прогноз, залежно від групи ризику:
- Низький. Основні методи лікування – спостереження, хірургічна операція. Рівень виживання – більше 95%.
- Проміжний. Основні методи лікування – хірургічна операція, хіміотерапія. Рівень виживання – більше 90%.
- Високий. Основні методи лікування – хірургічна операція, хіміотерапія, високодозована хіміотерапія з трансплантацією кісткового мозку, імунотерапія, променева терапія. Рівень виживання – менше 60%.
Коефіцієнт виживання для груп низького та помірного ризику становить близько 90%. Історично склалося так, що коефіцієнт виживання групи високого ризику становив 15%. З використанням більш інтенсивнішої терапії на сьогоднішній день цей коефіцієнт збільшився до 50%. А недавнє рандомізоване дослідження показало, що інтенсивна терапія у поєднанні з імунотерапією призвела до збільшення виживаності до 66%.
У пацієнтів із захворюванням високого ризику ймовірність рецидиву достатньо висока (більше 50%). Для пацієнтів із захворюванням низького ризику ризик рецидиву становить всього 5–15%. Найчастіше рецидив відбувається у перші 2 роки після завершення лікування. За відсутності ознак захворювання через 5 років після завершення лікування рецидив трапляється рідко. Після лікування пацієнтам необхідно регулярно проходити обстеження в рамках диспансерного спостереження на предмет рецидиву.
Лікування нейробластоми залежить від віку дитини, розташування пухлини, її особливостей (генних змін та гістологічних характеристик) та стадії захворювання і групи ризику рецидиву.
Сучасне лікування нейробластоми
Варіанти лікування нейробластоми:
- Спостереження.
- Хірургічна операція.
- Хіміотерапія.
- Високодозована хіміотерапія з трансплантацією кісткового мозку.
- Імунотерапія.
- Променева терапія.
- Участь в клінічних дослідженнях.
Щодо наймолодших пацієнтів із групи низького ризику може бути обрана тактика спостереження замість активного лікування. У деяких випадках нейробластома може зникати самостійно (регресія). Однак це трапляється рідко, і пацієнтам потрібний дуже ретельний моніторинг щодо можливого прогресування пухлини.
Якщо можливо, для видалення пухлини проводять хірургічну операцію. Щоб гарантувати повне видалення всіх злоякісних клітин, разом з пухлиною видаляють невелику кількість здорових оточуючих тканин. Пацієнтам з єдиним пухлинним осередком за відсутності поширення може бути проведена лише хірургічна операція. Однак, у деяких випадках повністю видалити пухлину неможливо, особливо при метастатичній нейробластомі. Тоді потрібне додаткове лікування.
Хіміотерапія – основний метод лікування нейробластоми, особливо в групах проміжного і високого ризику захворювання. Хіміотерапевтичні препарати знищують ракові клітини або зупиняють їх ріст та розмноження. Більшість хіміотерапевтичних препаратів вводяться шляхом ін’єкцій, але деякі препарати можуть призначатися перорально. При захворюванні високого ризику хіміотерапію, як правило, призначають перед хірургічною операцією для зменшення розміру пухлини. Крім того, хіміотерапія часто призначається після операції для знищення пухлинних клітин, що залишилися, і запобіганню рецидиву. Хіміотерапевтичними препаратами, що часто використовуються для лікування нейробластоми, є карбоплатин, циклофосфамід, доксорубіцин, етопозид, топотекан, цисплатин і вінкристин.
При метастатичній нейробластомі та захворюваннях високого ризику часто використовується високодозована хіміотерапія з наступною аутологічною трансплантацією стовбурових клітин (пересадка кісткового мозку). При використанні даного методу на початкових етапах лікування у пацієнта відбирають власну стовбурові клітини, які зберігаються для подальшої трансплантації. Після початкового лікування (як правило, після хіміотерапії та хірургічної операції) застосовують дуже високі дози хіміотерапії, щоб знищити всі злоякісні клітини, що залишилися. Потім пацієнту пересаджують власні здорові стовбурові клітини, щоб урятувати кістковий мозок від впливу високодозованої (мієлоаблятивної) терапії.
Для лікування нейробластоми високого ризику у поєднанні з іншими методами терапії часто використовується променева терапія. Оскільки такі пухлини вражають важливі органи, анатомічні структури та кровоносні судини, їх не вдається повністю видалити під час хірургічної операції, тому для знищення злоякісних клітин, що залишилися в пухлинному вогнищі, та лікування метастазів призначають променеву терапію.
Ретиноїди, такі як 13-цис-ретиноєва кислота (ізотретиноїн), знижують ризик рецидиву після лікування у дітей з нейробластомою високого ризику, особливо коли їх призначають у комплексі з імунотерапією. Введення 13-цис-ретиноєвої кислоти в комбінації з різними типами хіміотерапевтичних лікарських засобів, імунотерапевтичних засобів, а саме моноклональних антитіл, і таргетних лікарських засобів вивчається в ряді клінічних досліджень.
Імунотерапія на основі анти-GD2 моноклональних антитіл в даний час у розвинених країнах розглядається як стандарт лікування пацієнтів групи високого ризику, які досягли відповіді на тлі індукційної хіміотерапії. Ефективність моноклональних антитіл ch14.18 підтверджена в рамках проспективного рандомізованого дослідження III фази, організованого Дитячою онкологічною групою в США (препарат «Динутуксимаб»), та ретроспективного аналізу великої групи пацієнтів у дослідженнях Європейської групи з лікування нейробластоми (SIOPEN – препарат «Динутуксимаб бета»).
Отримані дані після гістологічних та молекулярно-генетичних досліджень пухлинних клітин дозволяє визначити особливості, які відрізняють клітини нейробластоми від нормальних клітин та може допомогти знайти нові методи лікування цього захворювання. Нові препарати, які діють на клітини нейробластоми більш прицільно, ніж стандартні хіміопрепарати, наразі активно вивчаються. Наприклад, лікарі зараз вивчають ліки, які впливають на шляхи харчування клітин нейробластоми, такі як кризотиніб (Xalkori) та alisertib (MLN8237). Також проходять випробування такі таргетні препарати: бортезоміб, вориностат, темсіролімус, бевацизумаб, ніфуртімокс та DMFO.
Моноклональне антитіло динутуксимаб (Unituxin®), яке спрямоване на мішень GD2, що міститься в клітинах пухлини, тепер застосовується для лікування дітей з агресивною нейробластомою. Цей препарат допомагає клітинам імунної системи знаходити та знищувати ракові клітини. На даний момент проводяться клінічні випробування кількох інших антитіл, націлених на GD2.
Декілька протиракових вакцин також вивчаються для лікування нейробластоми. При цьому пацієнту вводять модифіковані клітини пухлини чи інші речовини, щоб змусити власну імунну систему дитини атакувати злоякісні клітини. Ці методи лікування знаходяться на ранніх стадіях клінічних випробувань.
Т-клітинна терапія CAR – це багатообіцяючий новий спосіб отримання власних імунних клітин пацієнта, які називають Т-клітинами (білі кров’яні тільця) для боротьби з раком шляхом модифікації їх у лабораторних умовах, щоб вони могли знайти та знищити ракові клітини. Т-клітини модифікуються для визначення специфічних ракових клітин шляхом додавання штучного рецептора (так званого химерного рецептора антигену або CAR). У ході дослідження вдалося створити Т-клітини CAR для впливу на мішень GD2 клітини нейробластоми. Ви можете дізнатись більше про ці клінічні випробування у свого лікаря. В деяких випадках – участь в клінічних дослідженнях – це єдиний шанс на порятунок життя дитини.
У кожному окремому випадку рішення про комбінацію тих чи інших методик лікування приймається спільно командою спеціалістів. Завдяки такому підходу нам вдається досягти високого рівня виживання пацієнтів, навіть у найскладніших випадках. Для лікування епендимоми залучаються вузькопрофільні експерти, які тісно взаємодіють між собою. Постійна комунікація дозволяє швидко та ефективно приймати рішення щодо коригування схеми лікування, якщо в цьому виникає термінова необхідність, відстежувати результати операції та стан здоров’я маленького пацієнта.